发布日期:2026-03-25 浏览次数:
人类免疫缺陷病毒1型以其精密的基因调控网络著称。在不足10 kb的紧凑基因组内,它通过宿主剪接体的复杂加工,产生超过40种mRNA异构体,编码至少9种病毒蛋白——这几乎将编码能力发挥到了极致。然而,这个“寸土寸金”的基因组,是否还隐藏着未被发现的RNA物种?

研究团队首次发现,HIV-1感染的细胞会产生一种病毒编码的环状RNA,命名为circHIV。这种环状RNA能够结合病毒关键转录激活因子Tat蛋白,显著增强HIV-1启动子的转录活性,形成一个正反馈回路,加速病毒基因表达。这一发现揭示了HIV生命周期中一个此前被完全忽视的调控层面,为理解病毒致病机制和开发新型抗病毒策略开辟了新方向。
环状RNA是一类共价闭合的单链RNA分子,没有5帽和3 poly(A)尾,比线性RNA更稳定。最初在类病毒和丁型肝炎病毒中发现,如今已知环状RNA在真核细胞中广泛存在,部分具有海绵吸附microRNA、结合蛋白或翻译成多肽的功能。
在病毒学领域,EBV、KSHV、HPV等DNA病毒已被报道编码环状RNA。SARS-CoV-2、RSV和HCV等RNA病毒也产生病毒环状RNA。但逆转录病毒是否编码环状RNA,此前从未被探索。
HIV-1的转录本经过宿主剪接体广泛剪接,剪接位点的存在暗示了反向剪接产生环状RNA的可能性。本研究正是从这个角度切入,寻找HIV-1感染细胞中可能存在的病毒环状RNA。
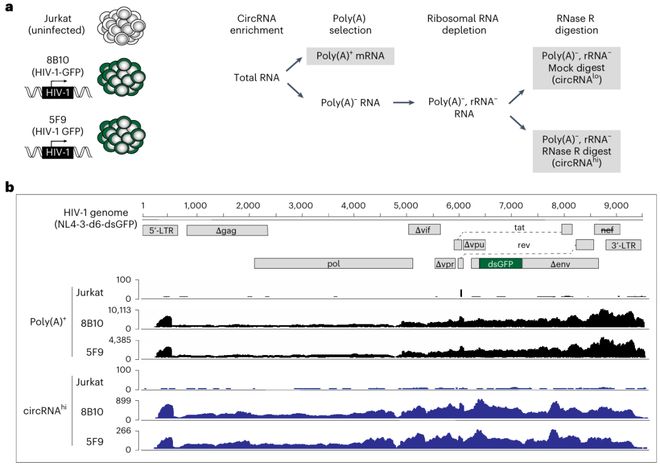
研究团队首先对HIV-1感染的Jurkat T细胞克隆进行环状RNA富集测序。通过去除poly(A) RNA、核糖体RNA,并用RNase R消化线性RNA,富集环状转录本后进行高通量测序。
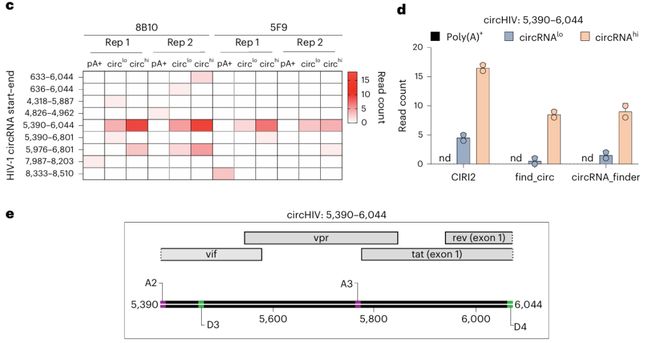
生物信息学分析在HIV-1基因组上鉴定出9个推定的病毒环状RNA,其中一个跨越核苷酸5,390-6,044的环状RNA在RNase R处理后富集最显著,且在多个感染细胞系中稳定存在。三个独立的环状RNA发现工具(CIRI2、find_circ、circRNA_finder)均鉴定出同一物种,将其命名为circHIV。
circHIV位于HIV-1基因组的中心区域,覆盖vpr、tat和rev的部分序列,上游为A2剪接受体,下游为D4剪接供体,符合反向剪接产生环状RNA的特征。
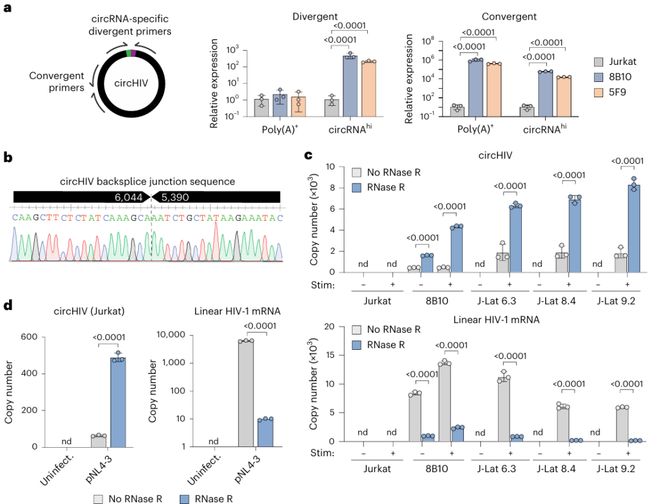
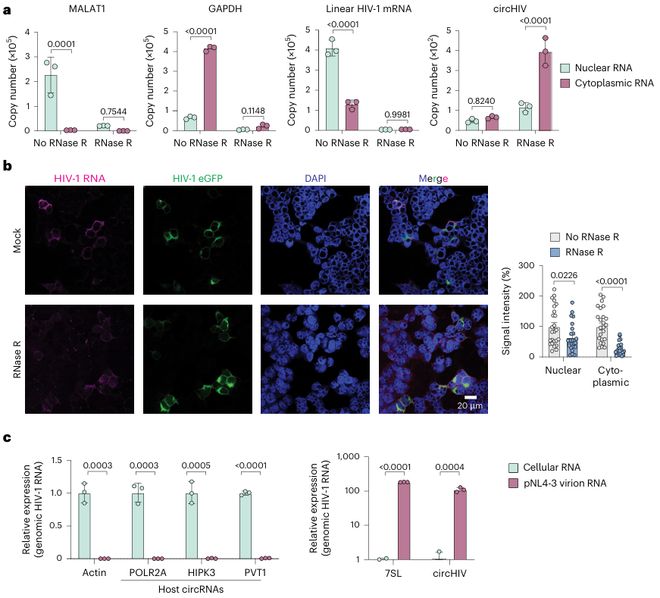
为验证circHIV的真实性,研究团队设计了跨反向剪接接头的发散引物。RT-qPCR证实,circHIV在RNase R处理后显著富集,而线 mRNA则被降解。Sanger测PG中国电子技术有限公司序确认了预期的反向剪接接头序列。
Northern blot进一步证实,circHIV以约655 nt和342 nt两种异构体形式存在,且对RNase R具有抗性。较小的异构体由D3和A3剪接位点之间的内部正向剪接产生。
将包含剪接位点的HIV-1片段克隆至表达质粒后,转染细胞同样检测到两种circHIV异构体,而缺乏侧翼序列的对照质粒则不产生,证实circHIV通过反向剪接产生。
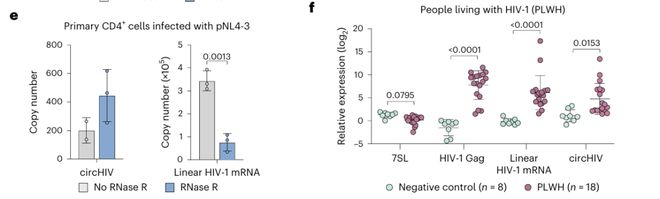
重要的是,circHIV不仅在Jurkat、293T、THP-1、HeLa等多种HIV-1感染细胞系中检出,还在原代CD4+ T细胞和18名HIV-1感染者的血浆样本中稳定存在。这是病毒环状RNA首次在患者血浆中被检测到,提示其可能作为潜在的生物标志物。
亚细胞分级显示,circHIV分布于细胞核和细胞质,但主要富集于细胞质,与主要定位于核的线 mRNA形成对比。RNA-FISH进一步证实了这一分布模式。
更令人惊讶的是,病毒颗粒纯化实验表明,circHIV被选择性包装进HIV-1病毒颗粒。与宿主环状RNA(circPOLR2A、circHIPK3、circPVT1)几乎不进入病毒颗粒不同,circHIV在病毒颗粒中的丰度接近已知被包装的7SL RNA。进一步的生信分析显示,约30%的病毒颗粒环状RNA注释到HIV-1基因组,表明多种病毒环状RNA被选择性包装。
这一发现暗示,circHIV可能在病毒进入新细胞后立即发挥功能,无需等待前病毒整合。
为探究circHIV的功能,研究团队设计了靶向其反向剪接接头的shRNA和CRISPR-Cas13d系统。
shRNA敲低circHIV后,HIV-1感染细胞的GFP阳性比例和平均荧光强度均显著下降,而线 mRNA水平不受影响。Cas13d介导的敲低同样导致GFP阳性细胞减少约1.5倍。
相反,体外合成的circRNA转染过表达实验中,circHIV使GFP阳性细胞增加约1.5倍,效果与外源性Tat mRNA相当。时间进程分析表明,circHIV不影响病毒进入、逆转录和整合,而是在转录阶段发挥增强作用。
荧光素酶报告基因实验进一步证实,circHIV增强HIV-1 LTR启动子活性,且与Tat协同作用,使转录活性显著高于Tat单独处理或与对照RNA共转染。
RNA免疫沉淀实验显示,抗Tat抗体能显著富集circHIV,而线 RNA不被富集。已知的Tat结合宿主转录本FADD和ISG20作为阳性对照被富集,阴性对照HPRT和宿主环状RNA则不被富集。
体外链霉亲和素pull-down实验证实,生物素标记的circHIV能直接结合纯化的Tat蛋白,而circ-mCherry和线 RNA则不能。通过分段替换,研究将Tat结合区域定位到circHIV的第93-188位核苷酸。
值得注意的是,circHIV与TAR RNA对Tat的结合互不竞争,提示二者可能结合Tat的不同结构域或协同作用。RNA二级结构预测显示,circHIV与线 RNA采取截然不同的构象,这可能解释了二者对Tat结合能力的差异。
本研究首次揭示,逆转录病毒HIV-1编码环状RNA,且这种环状RNA通过结合病毒关键转录激活因子Tat,增强HIV-1转录,形成一个正反馈回路。
存在性:HIV-1感染细胞产生病毒编码的环状RNA circHIV,在多种细胞系、原代细胞和患者血浆中检出。
机制:circHIV直接结合Tat蛋白,与TAR协同但不竞争,通过独特的RNA拓扑结构实现特异性结合。
揭示新的调控层次:环状PG中国电子技术有限公司RNA作为病毒转录的“隐形加速器”,是HIV-1基因调控的 overlooked layer。
治疗潜力:靶向circHIV或其与Tat的相互作用,可能成为抑制HIV-1转录的新策略。
正如研究者所言:“circHIV的发现揭示了环状RNA作为转录调控因子的新功能,为理解HIV-1致病机制和开发抗病毒疗法开辟了新方向。”