发布日期:2026-02-08 浏览次数:
【解析】 先根据题意,推断出W是Hale Waihona Puke Baidui,X是C,Y是Al,Z是S。A项,LiCl中的Li不满足8电子稳定结构,故A错误;B项,碳元素和氢元素可形成C2H2、C6H6、C8H8等多种原子比为1∶1的化合物;C项,Al与强酸、强碱都能反应放出氢气;D项,碳元素和硫元素能形成CS2。
3.(1)(2012·福建高考)元素M的离子与NH所含电子数和质子数均相同,则M的原子结构示意图为________。
【解析】A项,16O2与18O2都是氧气单质;B项,16O与18O核外均有8个电子,核外电子排布方式相同;C项,化学变化中元素原子的个数和种类不变;D项,标准状况下,1.12 L16O2和1.12 L18O2的物质的量均为0.05 mol,含氧原子个数均为0.1NA。
(2011·课标全国卷)短周期元素W、X、Y和ZPG中国电子技术有限公司的原子序数依次增大。元素W是制备一种高效电池的重要材料,X原子的最外层电子数是内层电子数的2倍,元素Y是地壳中含量最丰富的金属元素,Z原子的最外层电子数是其电子层数的2倍。下列说法错误的是()
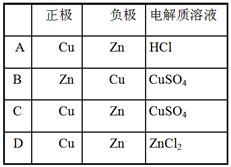
5.已知A、B、C、D是中学化学中常见的四种不同多核粒子,它们之间存在如下关系:
(1)如果A、B、C、D均是10电子的粒子,请写出:A的电子式_____;D的电子式_____。
(1)同种元素可以有若干种不同的核素,也可以只有一种核素,有多少种核素就有多少种原子。
【解析】 根据Y原子的L层电子数为a+b,M层电子数为a-b知a+b=8,再根据X原子次外层电子数为b,可知b=2,则a=6,进而确定X为氧(O),Y为硅(Si)。两元素形成SiO2,SiO2为酸性氧化物,可与NaOH反应。
2.(2013·上海高考)230Th和232Th是钍的两种同位素,232Th可以转化成233U。下列有关Th的说法正确的是()
2.了解原子构成。了解原子序数、核电荷数、质子数、中子数、核外电子数以及它们PG中国电子技术有限公司之间的相互关系。(高频)
3.(2010·山东高考)16O和18O是氧元素的两种核素,NA表示阿伏加德罗常数,下列说法正确的是()
1.据2012年2月6日中新网报道,嫦娥二号月球探测器获得了7m分辨率全月球影像图,该月球探测器使用钚元素的同位素电池来提供稳定、持久的能源。下列关于Pu的说法正确的是()
【解析】Pu和Pu的质量数之差为2,A错误;Pu和Pu的质子数均为94,中子数(或质量数)不同,属于钚的两种核素,B正确;Pu的中子数与质子数之差为50,C错误;Pu和Pu互为同位素,D错误。
【解析】232Th、230Th的质量数分别是232,230,A项错误;元素的相对原子质量是由各种同位素的相对原子质量与百分含量求得的平均值,B项错误;同位素的物理性质可以不同,但化学性质相同,D项正确,化学变化是生成新物质的变化,原子不变,而C项的原子发生变化。
【解析】I与I互为同位素,二者的化学性质相同;I的原子序数为53,原子核外电子数为53,中子数为131-53=78,则I的原子核内中子数多于质子数。
分析题中某些元素原子的核外电子排布特点―→联想核外电子排布规律―→确定某原子的核外电子排布―→确定元素。
4.(2014·鞍山模拟)短周期元素X和元素Y,元素X原子的最外层电子数为a,次外层电子数为b;元素Y原子的M层电子数为(a-b),L层电子数为(a+b),则X、Y两元素形成的化合物可能具有的性质是()
(3)质子数相同的微粒不一定属于同一种元素如Ne、HF、H2O、NH3、CH4等。
(2011·海南高考)I是常规核裂变产物之一,可以通过测定大气或水中I的含量变化来监测核电站是否发生放射性物质泄漏。下列有关I的叙述中错误的是()